《柳叶刀》子刊:疾病控制率达95%!肠菌移植联合免疫疗法或可提高这类结直肠癌的治愈率
2023-11-24
阅读(2500)
结直肠癌(CRC)是全球发病率第三、死亡率第二的恶性肿瘤。我国结直肠癌的发病率和死亡率均保持上升趋势。2020年中国癌症统计报告显示:我国结直肠癌发病率、死亡率在全部恶性肿瘤中分别位居第2和第5位,其中2020年新发病例55.5 万,死亡病例28.6万[1]。其中,城市远高于农村,且结肠癌的发病率上升显著。因此,对于结直肠癌的治疗是目前迫切需要解决的问题。
近日,武汉大学人民医院临床肿瘤科,陈永顺团队探讨了肠道菌移植与替雷利珠单抗和呋喹替尼联合治疗难治性MSS mCRC的有效性和安全性,并发现其作为三线或以上治疗可显著提高难治性MSS mCRC患者的生存率且安全性可控,为该患者群体提供了一种有价值的新治疗选择,最新研究成果发表在LANCET子刊《eClinicalMedicine》上,影响因子15.1。免疫疗法使癌症的治疗发生了革命性的变化。然而,微卫星稳定(MSS)转移性结直肠癌(mCRC)患者对PD-1抑制剂的反应较低。抗血管生成治疗可提高抗pd -1的疗效,但仍不能满足临床需要。越来越多的证据显示肠道微生物组与抗pd -1疗效之间有密切关系。本研究旨在探讨肠道微生物群移植(FMT)联合替利单抗和呋喹替尼治疗难治性MSS mCRC的疗效和安全性。此项实验为II期临床试验,MSS mCRC患者接受FMT +替雷利珠单抗和呋喹替尼作为三线或以上治疗。主要终点为无进展生存期(PFS)。次要终点为总生存期(OS)、客观缓解率(ORR)、疾病控制率(DCR)、缓解持续时间(DoR)、临床获益率(CBR)、安全性和生活质量。收集粪便和外周血进行探索性生物标志物分析。肠菌移植前,患者口服抗生素(万古霉素500 mg和新霉素100 mg,每6小时)72小时。在移植前15小时,口服聚乙二醇腹泻溶液用于肠道清洁准备和菌群定植。然后通过口服定制FMT胶囊进行FMT治疗,剂量为30粒/天(相当于3瓶40毫升肠道微生态液体制剂),连续3天,3周为一个周期,持续4-18个周期。
呋喹替尼每天口服一次,起始剂量为5mg,持续服用2周,停1周,替雷利珠单抗200 mg每3周静脉注射一次,直到不可接受的毒性,临床获益丧失,疾病进展,死亡,完成18个研究治疗周期,或应患者要求停止治疗。20名患者入选。中位随访期13.7个月。中位PFS为9.6个月。中位OS为13.7个月。中位生存时间为8.1个月。ORR为20%。DCR为95%。CBR为60%。有12例患者被归类为治疗起效,应答者(PFS≥6个月),8例患者被归类为效果欠佳,非应答者(PFS<6个月)。没有发生与治疗相关的死亡。应答者中变形杆菌和毛螺菌科的种类较多,放线杆菌和双歧杆菌的丰度较低。这提示肠道微生物可能在FMT联合治疗中发挥重要作用。FMT联合替雷利珠单抗和呋喹替尼作为三线或以上治疗在难治性MSS mCRC中显示出更高的生存率和可管理的安全性,为该患者群体提供了有价值的新治疗选择。
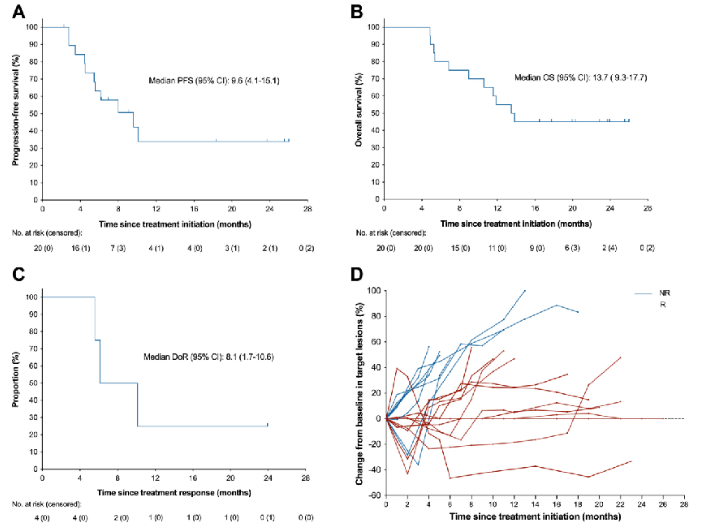
图1:肿瘤反应与Kaplan-Meier曲线
截至2023年7月,中位随访期为13.7个月(范围4.9-26.0),中位无进展生存期为9.6个月(95%可信区间4.1-15.1),中位总生存期为13.7个月(95%可信区间9.3-17.7)。
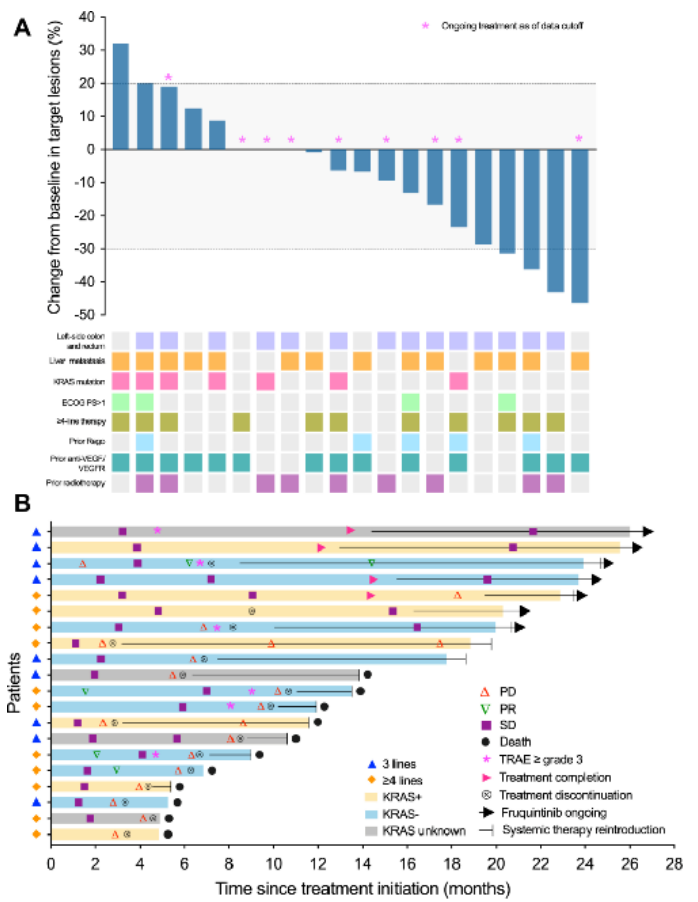
患者被标记为有效者(PFS≥6个月;n=12)和无应答者(PFS<6个月;n=8),CBR达到60%(95%可信区间36.1~80.9)。中位治疗周期为7.5个周期(3-18个周期),60%的患者靶区缩小。疾病控制率为95%,临床获益率为60%。
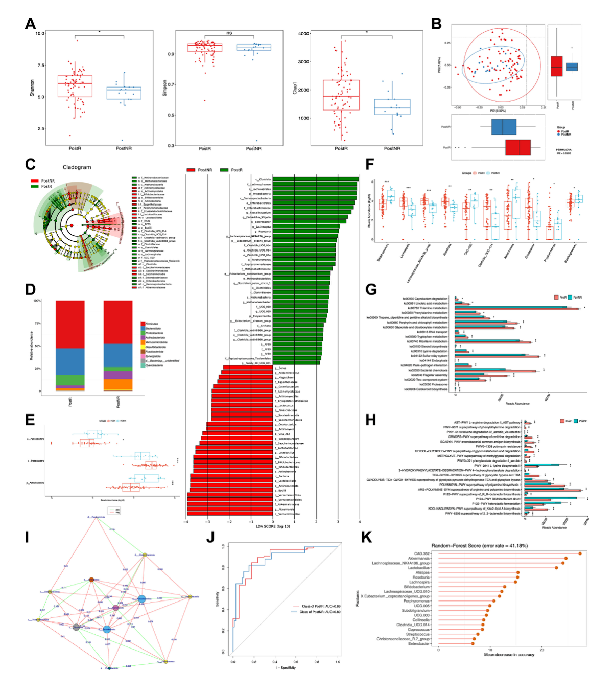
图3:应答者和无应答者在研究治疗后的肠道微生物群有显著差异
应答者和无应答者在α和β多样性方面观察到显著差异。在应答者中,变形杆菌在门的水平上增加,而在无应答者中放线杆菌和髌骨菌明显更丰富。在应答者中观察到肠杆菌属、埃希氏志贺氏菌属、粪肠杆菌属等显著增加以及重要生物过程的功能富集,如糖酵解、TCA 循环、氨基酸代谢、鞭毛组装和细菌趋化性等。
来源: 转载自微信公众号 仅供学习 侵删






